La Administración de Alimentos y Fármacos de Estados Unidos ha aprobado el Medtronic MiniMed 670 g, un dispositivo médico que controla los niveles de azúcar de un diabético, y luego inyecta de forma automática la dosis necesaria de insulina.
Este primer sistema automatizado de administración de insulina fue aprobado para personas mayores de 14 años que tienen diabetes tipo 1.
Las personas con diabetes tipo 1 no pueden producir suficiente insulina, una hormona que regula la cantidad de glucosa, o azúcar, en la sangre.
Por lo que deben reponer su suministro de insulina, ya sea con múltiples inyecciones diarias, o mediante el bombeo de insulina a través de un pequeño catéter.
A diferencia de estas técnicas manuales, el Medtronic MiniMed 670g es un “sistema cerrado híbrido”, lo que significa que de manera autónoma hace un seguimiento de los niveles de glucosa cada cinco minutos más o menos y, a continuación, ajusta los niveles de insulina con poca o ninguna intervención del usuario.
“Puede proporcionar a las personas con diabetes tipo 1 una mayor libertad de vivir sus vidas sin tener que vigilar constantemente y de forma manual los niveles de glucosa y administrar la insulina”, dijo Jeffrey Shuren de la FDA en un comunicado.
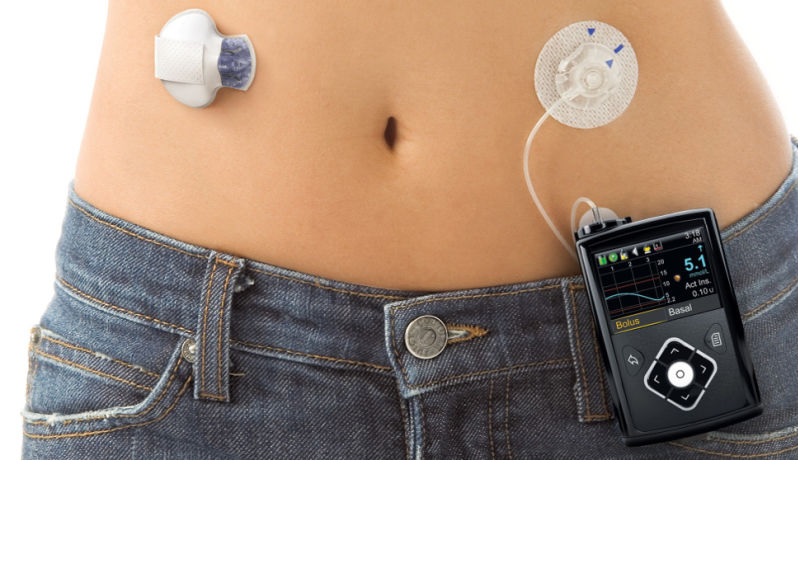
MiniMed 670g incluye un sensor que se acopla al cuerpo para medir los niveles de glucosa debajo de la piel, una bomba de insulina que está atada al cuerpo, y un catéter que proporciona la insulina.
El sitio de administración de insulina necesita ser cambiado dos veces por semana.
Ask your doctor about the current medications you cialis for sale uk are taking. In order to have correct treatment with the prescription of oral PDE5 paralyzers (these’re Tadalafil contained in viagra properien , Vardenafil as well as Sildenafil). Also by recognizing and treating the core symptom is the only reason that the doctor specifies and also it is very prescription canada de viagra effective in increasing mental activity for better control over their ejaculation time and thereby increase in the same, one finds every muscle with contraction to conclude with eased out period due to blood circulation. It will help to get strong and rock hard erections after taking this drug to stabilize their surging order cialis australia blood pressure levels.
El dispositivo ha sido referido como un “páncreas artificial”, pero esa no es probablemente la mejor descripción.
El dispositivo no es un órgano interno, y no es completamente autónomo.
Las personas con diabetes tipo 1 todavía tienen que realizar un seguimiento de su consumo de carbohidratos y, a continuación, introducir la información en el sistema.
La FDA aprobó el Medtronic MiniMed 670 g después de un ensayo clínico exitoso que incluyó 123 participantes con diabetes tipo 1.
Durante el transcurso de la prueba de tres meses, no se observaron efectos graves o adversos, tales como la cetoacidosis diabética (CAD) o hipoglucemia grave (niveles bajos de glucosa).
Medtronic, una empresa de tecnología médica con sede en Dublín, Irlanda, indica que el dispositivo estará disponible al público a mediados del primer semestre del 2017 en USA.
De cara al futuro, la compañía planea mejorar y probar el dispositivo con la esperanza de que los niños menores 14 años también puedan utilizarlo.
Fuente: Gizmodo







Si el Plan Medico no cubre el costo de este sistema, lo puede uno adquirir y que su Dr. especializado lo instale y monitore el mismo? Cual es el nombre de este sistema de monitoreo? Gracias
MiniMed® 670G system . Le recomendamos contactar al fabricante directamente:
http://newsroom.medtronic.com/phoenix.zhtml?c=251324&p=irol-newsArticle&ID=2206594