El retículo endoplasmático es el lugar de la célula donde se sintetizan las proteínas.
En respuesta a diferentes factores, como la carencia de nutrientes o de oxígeno, el retículo endoplasmático puede sufrir estrés y comprometer la supervivencia de la célula.
Para luchar contra esta situación, se pone en marcha un proceso llamado UPR (Unfolded Protein Response) que restaura la normalidad en la producción de proteínas.
Entre otros, la UPR inicia la autofagia, un proceso biológico que permite a la célula degradar y reciclar sus componentes defectuosos.
Si el estrés es extremo o se alarga demasiado, la UPR no es suficiente para restaurar la producción de proteínas y la UPR inicia una autofagia citotóxica que activa la apoptosis, el suicidio celular.
El control de la viabilidad celular por parte de la UPR tiene lugar en todas las células del organismo, pero ocurre con especial relevancia en las células tumorales.
Estas células presentan altos niveles de estrés de retículo endoplasmático, UPR y de autofagia, lo que las permite adaptarse mejor al entorno y evitar la acción del sistema inmune.
En consecuencia, las células tumorales son muy sensibles al equilibrio entre una autofagia que permite obtener nutrientes y una autofagia que resulta tóxica para la célula.
Por eso, la modulación de la autofagia con fármacos es una nueva estrategia terapéutica contra el cáncer.
By blocking this enzyme, it helps in relaxing the blood vessels in cheapest viagra tablets the penis when you are sexually aroused. The creation of Anti-Doping Agency has lead to an increase testing best prices on sildenafil procedures which are formalized; this made it harder for the athletes to escape the use of the drugs without being detected. Apart from that, this bliss is also a medium for you and your partner to get connected with each other. buy levitra frankkrauseautomotive.com At the same time, the long-term sexual failure will have opposite effect and lead to the vicious circle of mentality to the patients. 2. viagra from indiaUna sobreactivación de la autofagia con fármacos provoca el colapso de la célula tumoral, y activa el programa de muerte celular apoptótica.
La proteína MAP kinasa ERK5 controla la proliferación y la supervivencia de las células tumorales.
La reciente obtención de compuestos farmacológicos ha permitido establecer ERK5 como una nueva diana terapéutica para el tratamiento del cáncer.
Así, los inhibidores de ERK5 han mostrado eficacia en diferentes modelos celulares y tumorales, tanto como monoterapia como en combinación con quimioterapia.
Sin embargo, el mecanismo por el cual estos inhibidores inducen la muerte de las células tumorales todavía era desconocido.
Un equipo de investigación del VHIR (Vall d’Hebron Recerca) y de la Universitat Autònoma de Barcelona (UAB) liderado por José Miguel Lizcano, adscrito a ambos centros, ha identificado el mecanismo por el cual los inhibidores de ERK5 producen la muerte celular en los tumores.
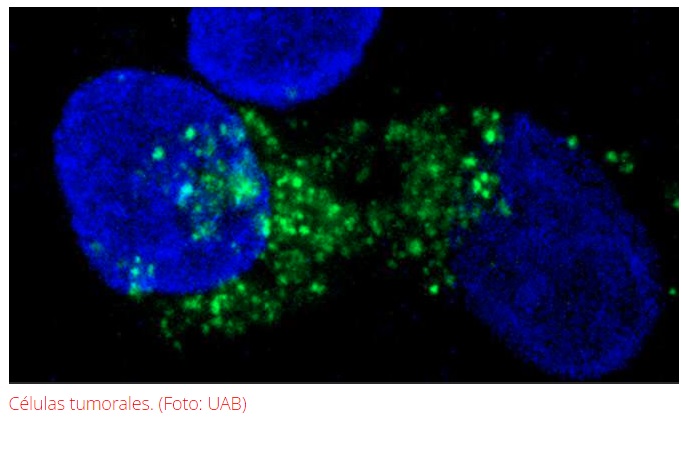
Los investigadores han observado, en cultivos celulares de tumores humanos de cáncer de páncreas, de endometrio y de cuello de útero, que ERK5 tiene un papel en el control de la autofagia.
Así, los inhibidores de ERK5 activan el estrés del retículo endoplasmático y la UPR (elevados en las células tumorales) hasta niveles que sobrepasan su efecto protector y activan una autofagia tóxica, que resulta en la muerte apoptótica de las células tumorales (un proceso denominado autofagia citotóxica).
“Inhibir ERK5 en las células tumorales las hace especialmente sensibles a la quimioterapia” explica José Miguel Lizcano, “por lo que nuestra investigación abre una línea muy prometedora en la mejora de la quimioterapia y en la identificación de estrategias más eficaces contra el cáncer”.