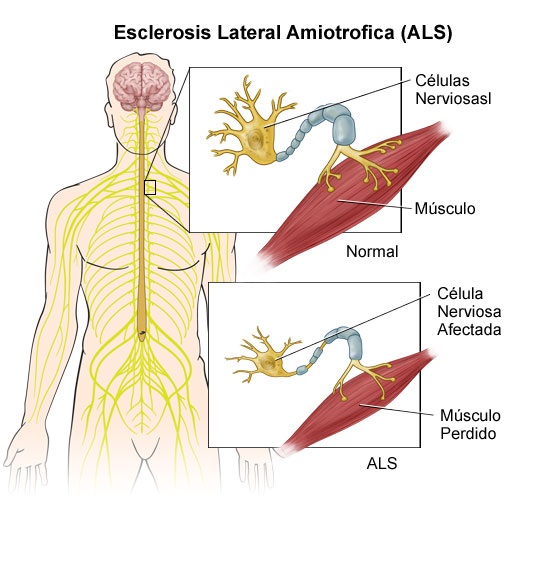
La Esclerosis Lateral Amiotrófica (ELA) provoca la pérdida de neuronas motoras y la parálisis de los músculos esqueléticos y, hasta ahora, no existe ninguna cura ni tratamiento efectivos.
Un estudio liderado por el Centro de Biomateriales e Ingeniería Tisular (CBIT) de la Universidad Politécnica de Valencia (UPV), en colaboración con el Instituto de Investigación Sanitaria La Fe (IIS La Fe), el Centro de Investigación Biomédica en Red (CIBER) y la Universidad de Zaragoza (Unizar) propone un novedoso enfoque para frenar la degeneración neuromuscular en pacientes con Esclerosis Lateral Amiotrófica.
En esta investigación, el equipo de la UPV, el CIBER, el IIS La Fe y la Unizar partió de la hipótesis de que el músculo esquelético puede tener una contribución activa en la patología de la enfermedad, y estableció el tejido muscular esquelético como una diana terapéutica para tratar la ELA.
En estudios previos, el equipo de la UPV ya demostró que el transportador de boro, NaBC1, después de su activación, potencia y acelera la reparación muscular.
Ahora los investigadores han corroborado su efectividad en un modelo de ratón de ELA, representativo del modelo de la variante familiar (genética) SOD1 de la enfermedad, que sobreexpresa el gen mutado humano de la proteína SOD1.
“Este modelo es el más estudiado para la realización de ensayos preclínicos previos a la investigación en humanos, debido a que recapitula la degeneración de las neuronas motoras inferiores, y la atrofia por denervación muscular ocurre antes de cualquier signo evidente de neurodegeneración”, explica Patricia Rico, investigadora del CBIT y miembro del CIBER de Bioingeniería, Biomateriales y Nanomedicina (CIBERBBN).
En su estudio, inyectaron un hidrogel de alginato cargado con boro (desarrollado en los laboratorios del CBIT) en los cuádriceps del modelo de ratón de ELA.
“Descubrimos que solo cuatro inyecciones del tratamiento administrado en el cuádriceps de ratones sintomáticos mejoraron significativamente la función motora.
Además, redujeron también eficazmente la atrofia muscular, retrasando el inicio evidente de los síntomas y prolongando la supervivencia de los ratones.
La activación de NaBC1 potenció los procesos de reparación muscular, lo que derivó en la reducción de varias características patológicas de los músculos afectados por la ELA y una disminución de la inflamación muscular junto con la activación de vías metabólicas musculares esenciales”, destaca Patricia Rico.
El equipo de la UPV, el consorcio CIBER y el IIS La Fe comprobó también que el tratamiento tenía un efecto modulador de la inflamación muscular y neuronal, mitigando la pérdida de neuronas motoras, lo que sugiere un efecto neuroprotector retrógrado.
“Estos hallazgos son muy relevantes para entender la influencia del tejido muscular en la progresión de la ELA, y constatan la idoneidad de establecer también al músculo esquelético como una diana terapéutica.
Con nuestro estudio, proponemos un enfoque novedoso para frenar la degeneración neuromuscular en la ELA, que podría complementar las terapias en uso existentes dirigidas a la muerte de las neuronas motoras.
Una posible terapia combinada de tratamientos dirigidos a frenar la inflamación de las motoneuronas junto con tratamientos dirigidos a favorecer la regeneración muscular podría tener más probabilidades de éxito para alargar y mejorar la calidad de vida de los pacientes que sufren esta terrible enfermedad”, destaca Juan Francisco Vázquez, investigador del IIS La Fe, coordinador de la Unidad de ELA del Hospital la Fe y miembro del CIBER de Enfermedades Raras (CIBERER).
Actualmente, el equipo de investigación está evaluando, en el mismo modelo de ratón de ELA, SOD1, un medicamento que es un compuesto de boro para proponer su reposicionamiento con una aplicación diferente a su indicación original.
“En este caso, si los resultados son positivos, se podría utilizar con la indicación terapéutica de regeneración del músculo esquelético.
El reposicionamiento de este fármaco supondría un avance significativo en sus fases regulatorias, y una gran ventaja para su uso en ensayos clínicos, reduciéndose también los tiempos hasta llegar a los pacientes de ELA”, destaca el Dr. Vázquez.
Fuente: UPV