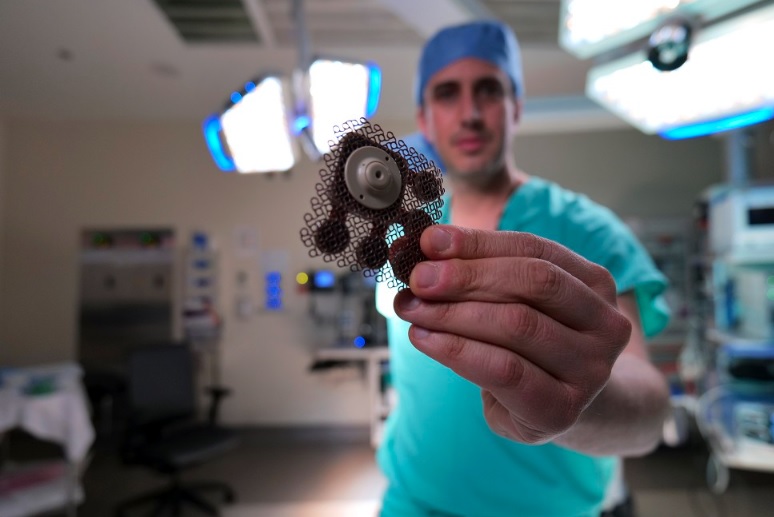
El dispositivo utiliza microburbujas para abrir la barrera hematoencefálica para tratar el glioblastoma en humanos.
Un impedimento importante para tratar el glioblastoma, un cáncer cerebral mortal, ha sido que la quimioterapia más potente no puede penetrar la barrera hematoencefálica para alcanzar el agresivo tumor cerebral.
Pero ahora, científicos de Northwestern Medicine informan los resultados del primer ensayo clínico en humanos en el que usaron un novedoso dispositivo de ultrasonido implantable en el cráneo para abrir la barrera hematoencefálica y penetrar repetidamente grandes regiones críticas del cerebro humano para administrar quimioterapia que fue inyectada por vía intravenosa.
El procedimiento de cuatro minutos para abrir la barrera hematoencefálica se realiza con el paciente despierto y los pacientes se van a casa después de unas horas.
Los resultados muestran que el tratamiento es seguro y bien tolerado, y algunos pacientes reciben hasta seis ciclos de tratamiento.
Este es el primer estudio que cuantifica con éxito el efecto de la apertura de la barrera hematoencefálica basada en ultrasonido sobre las concentraciones de quimioterapia en el cerebro humano.
La apertura de la barrera hematoencefálica condujo a un aumento de aproximadamente cuatro a seis veces en las concentraciones del fármaco en el cerebro humano, mostraron los resultados.
Los científicos observaron este aumento con dos poderosos medicamentos de quimioterapia diferentes, paclitaxel y carboplatino.
Los medicamentos no se usan para tratar a estos pacientes porque no cruzan la barrera hematoencefálica en circunstancias normales.
Además, este es el primer estudio que describe qué tan rápido se cierra la barrera hematoencefálica después de la sonicación.
La mayor parte de la restauración de la barrera hematoencefálica ocurre en los primeros 30 a 60 minutos después de la sonicación, descubrieron los científicos.
Los hallazgos permitirán la optimización de la secuencia de administración del fármaco y la activación por ultrasonido para maximizar la penetración del fármaco en el cerebro humano, dijeron los autores.
“Esto es potencialmente un gran avance para los pacientes con glioblastoma“, dijo el investigador principal, el Dr. Adam Sonabend, profesor asociado de cirugía neurológica en la Facultad de Medicina Feinberg de la Universidad Northwestern y neurocirujano de Northwestern Medicine.
La temozolomida, la quimioterapia actual utilizada para el glioblastoma, atraviesa la barrera hematoencefálica, pero es un fármaco débil, dijo Sonabend.
La barrera hematoencefálica es una estructura microscópica que protege al cerebro de la gran mayoría de los fármacos en circulación.
Como resultado, el repertorio de fármacos que pueden utilizarse para tratar enfermedades cerebrales es muy limitado.
Los pacientes con cáncer de cerebro no pueden ser tratados con la mayoría de los medicamentos que de otro modo son efectivos para el cáncer en otras partes del cuerpo, ya que estos no cruzan la barrera hematoencefálica.
La reutilización efectiva de medicamentos para tratar la patología cerebral y el cáncer requiere su administración al cerebro.
En el pasado, los estudios que inyectaron paclitaxel directamente en el cerebro de pacientes con estos tumores observaron signos prometedores de eficacia, pero la inyección directa se asoció con toxicidad como irritación cerebral y meningitis, dijo Sonabend.
Los científicos descubrieron que el uso de ultrasonido y la apertura de la barrera hematoencefálica basada en microburbujas es transitoria, y la mayor parte de la integridad de la barrera hematoencefálica se restablece dentro de una hora después de este procedimiento en humanos.
“Hay una ventana de tiempo crítica después de la sonificación cuando el cerebro es permeable a los medicamentos que circulan en el torrente sanguíneo”, dijo Sonabend, también miembro del Centro Oncológico Integral Robert H. Lurie de la Universidad Northwestern.
Estudios anteriores en humanos mostraron que la barrera hematoencefálica se restablece por completo 24 horas después de la sonicación del cerebro y, según algunos estudios en animales, el campo asumió que la barrera hematoencefálica está abierta durante las primeras seis horas más o menos.
El estudio de Northwestern muestra que esta ventana de tiempo podría ser más corta.
En otra primicia, el estudio informa que el uso de una nueva rejilla implantable en el cráneo de nueve emisores de ultrasonido diseñada por la compañía francesa de biotecnología Carthera abre la barrera hematoencefálica en un volumen de cerebro que es nueve veces más grande que el dispositivo inicial.
Esto es importante porque para que sea efectivo, este enfoque requiere la cobertura de una gran región del cerebro adyacente a la cavidad que queda en el cerebro después de la extirpación de los tumores de glioblastoma.
Los hallazgos del estudio son la base de un ensayo clínico de fase 2 en curso que los científicos están realizando para pacientes con glioblastoma recurrente.
El objetivo del ensayo, en el que los participantes reciben una combinación de paclitaxel y carboplatino administrados en el cerebro con la técnica de ultrasonido, es investigar si este tratamiento prolonga la supervivencia de estos pacientes.
Una combinación de estos dos medicamentos se usa en otros tipos de cáncer, que es la base para combinarlos en el ensayo de fase 2.
En el ensayo clínico de fase 1 informado en este documento, los pacientes se sometieron a cirugía para la resección de sus tumores y la implantación del dispositivo de ultrasonido. Comenzaron el tratamiento a las pocas semanas de la implantación.
Los científicos aumentaron la dosis de paclitaxel administrada cada tres semanas con la apertura de la barrera hematoencefálica basada en ultrasonido.
En subgrupos de pacientes, se realizaron estudios durante la cirugía para investigar el efecto de este dispositivo de ultrasonido en las concentraciones del fármaco.
La barrera hematoencefálica se visualizó y cartografió en el quirófano utilizando un tinte fluorescente llamado fluoresceína y mediante resonancia magnética obtenida después de la terapia de ultrasonido.
“Si bien nos hemos centrado en el cáncer de cerebro (para el cual hay aproximadamente 30 000 gliomas en los EE. UU.), esto abre la puerta para investigar nuevos tratamientos basados en medicamentos para millones de pacientes que padecen diversas enfermedades cerebrales”, dijo Sonabend.
Fuente: Northwestern Now